Laboratorio del corso di Biochimica del Metabolismo
Corso di Laurea in Biotecnologie
Produzione di una Proteina Ricombinante
- La proteina scelta per questa esercitazione è una molecola che, per
alcuni aspetti, ha rivoluzionato la ricerca biologica di questi ultimi anni.
Si tratta infatti di una proteina fluorescente (da cui il nome GFP) con un
fluoroforo costituito da residui amminoacidici modificati, capace di emettere
un segnale molto forte e quindi di essere visibile a bassissime concentrazioni.
Per queste caratteristiche, il gene che la codifica è largamente utilizzato
come gene reporter, per seguire il destino di vari componenti cellulari. La
GFP è stata isolata da una medusa, l'Aequorea victoria.
La proteina GFP (green fluorescent protein)

La medusa A. victoria bioluminescente grazie alla GFP |
Informazioni utili
La sua sequenza, dedotta dal cDNA, è costituita da 238 amminoacidi con un peso molecolare intorno ai 30 kDa. La sua struttura è eccezionalmente stabile dal punto di vista della temperatura e pH. Considerevole è anche la sua resistenza alla degradazione proteolitica.
Queste caratteristiche sono probabilmente una conseguenza della compattezza della sua struttura terziaria

Struttura tridimensionale della GFP. La
molecola è costituita da 11 beta strands che formano una particolare
struttura a cilindro, scoperta proprio in questa proteina, definita beta-can.
All'interno, in azzurro, è visibile una alfa-elica con il cromoforo
(in giallo) ad una estremità. Il cilindro ha un diametro di circa
30 Å ed una altezza di circa 40 Å. Cliccando la figura con
il mouse si apre il modello interattivo |
Per i più curiosi sono disponibili molte informazioni in rete, fra le quali una pagina dedicata dalla olimpus alle varianti della proteina ed ai suoi principali impieghi nello studio delle cellule. Le potenziali applicazioni della proteina e la conoscenza della sua struttura hanno favorito anche la creazione di mutanti aventi spettri di eccitazione ed emissione diversi e quindi in grado di essere impiegati simultaneamente.
La proteina che useremo nella nostra esercitazione è la variante SYFP (Super Yellow Fluorescent Protein)
La proteina che verrà prodotta in questa esercitazione è uno dei mutanti della GFP e presenta: una fluorescenza più intensa della
molecola di Aequorea e per questo è motivo definita con il termine di S-YFP
(S sta per super); una lunghezza d'onda di emissione massima compresa nell'intervallo fra 525nm e 550nm che gli conferisce un colore giallo, da cui S-Y-FP (Yellow); una spiccata sensibilità al pH, al variare del quale variano sia lo spettro di emissione e quello di assorbimento sia anche anche il valore massimo di emissione. Il mutante, inoltre, è stato ottimizzato nel nostro laboratorio per l'espressione in Chlamydomonas reinhardti,
cambiando alcune basi senza tuttavia alterare la sequenza della proteina. In
sostanza, alcuni codoni sono stati modificati per tener conto della frequenza
del loro uso nelle alghe (questa strategia serve a rendere più efficiente
l'espressione del gene in questo tipo di cellule).
La risposta al pH
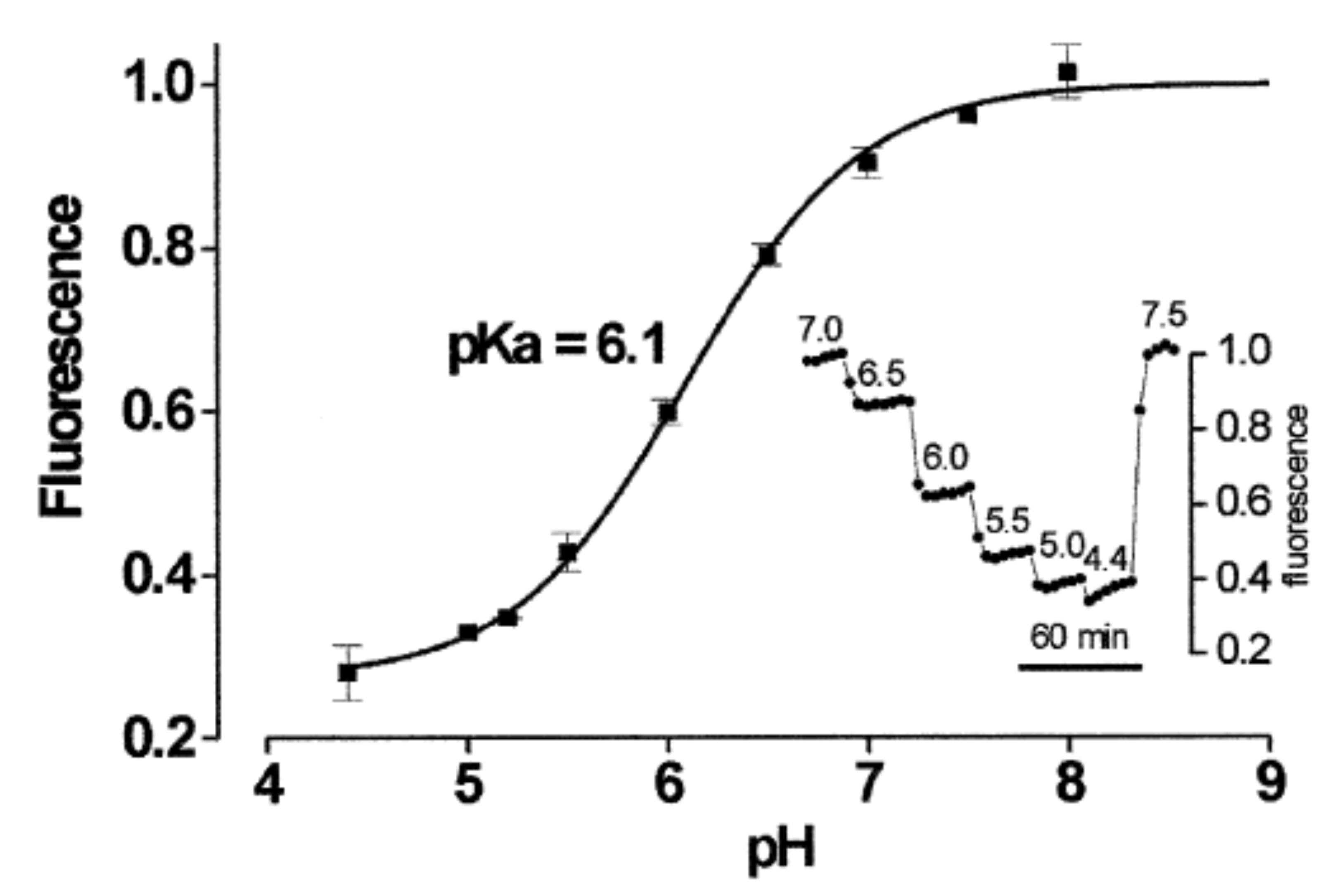
In alcune applicazioni biotecnologiche risulta estremamente utile l'espressione in vivo di una proteina in grado di cambiare uno o più parametri spettrofotometrici in risposta al variare dell'ambiente intracellulare. Sono state ottenute, per mutagenesi casuale seguita da screening delle proprietà spettrofotometriche, varianti delle proteine fluorescenti sensibili al variare del pH o del potenziale redox. L'espressione di queste proteine all'interno delle cellule o anche più specificatamente di alcuni organelli, consente di seguire, tramite microscopia in fluorescenza o fluorimetria, alcuni importanti processi cellulari o di selezionare, a seguito di mutagenesi, cellule che abbiano acquisito un fenotipo di interesse legato a questi parametri (es. i sovraccitati pH e potenziale redox). Nel caso specifico della nostra proteina è possibile fare una vera e propria "titolazione" seguendo l'intensità del segnale emesso al variare del pH della soluzione nella quale la nostra SYFP sarà immersa. Quello che ci aspettiamo di vedere sarà qualcosa di molto simile al grafico riportato qui di seguito:
Referenze:
Kremers GJ, Goedhart J, van Munster EB, Gadella TW Jr.
Biochemistry. 2006 May 30;45(21):6570-80.
Metzger F, Repunte-Canonigo V, Matsushita S, Akemann W, Diez-Garcia J, Ho CS, Iwasato T, Grandes P, Itohara S, Joho RH, Knöpfel T.
Eur J Neurosci. 2002 Jan;15(1):40-50.